DUOLife
BEOBACHTUNGSSTUDIE ZUR ERSTLINIENTHERAPIE BEI PATIENTINNEN MIT FORTGESCHRITTENEM ODER RÜCKFÄLLIGEM GEBÄRMUTTERSCHLEIMHAUTKREBS
Die DUOLife-Studie ist eine sogenannte nicht-interventionelle Beobachtungsstudie. Das bedeutet: Die Patientinnen erhalten eine bereits geplante oder begonnene und zugelassene Therapie – es werden weder Therapien oder sonstige Interventionen durch die Studie vorgegeben, noch angepasst. Mit dieser Studie sollen lediglich Daten zur Erfahrungen aus dem Behandlungsalltag in Deutschland (Real-World-Daten) gesammelt werden: Wie wirksam und verträglich ist die Erstlinientherapie mit Carboplatin, Paclitaxel und Durvalumab gefolgt von einer Erhaltungstherapie aus Durvalumab – allein oder in Kombination mit Olaparib – bei Patientinnen mit fortgeschrittenem oder erneut aufgetretenem (rezidivierendem) Gebärmutterschleimhautkrebs (auch Endometriumkrebs genannt)?
Was wird in dieser Studie untersucht?
Endometriumkrebs im fortgeschrittenen Stadium (FIGO III oder IV) oder bei einem Rückfall wird heute zunehmend mit einer Chemotherapie in Kombination mit einer Immuntherapie behandelt. In dieser Studie wird untersucht, wie gut eine solche Therapie im Behandlungsalltag funktioniert. Denn große klinische Studien haben den Nutzen dieser Therapien bereits an hunderten Patientinnen bestätigt. Nun soll die Wirkung auch außerhalb von großen klinischen Studien im normalen Behandlungsalltag in Deutschland untersucht werden. Dies ermöglicht es, die Wirkung der Therapie auch bei den Patientinnen zu untersuchen, die nicht an den klinischen Studien teilgenommen haben oder daran nicht teilnehmen konnten.
Durvalumab ist ein sogenannter Immun-Checkpoint-Inhibitor. Das Medikament hilft dem körpereigenen Immunsystem, Krebszellen besser zu erkennen und zu bekämpfen. Viele Tumorzellen werden durch ein bestimmtes Eiweiß (PD-L1) auf ihrer Oberfläche vor dem Angriff durch Immunzellen geschützt. Durvalumab blockiert diesen Schutzmechanismus, sodass das Immunsystem die Krebszellen angreifen kann. Die Kombination aus Chemotherapie und Immuntherapie kann sich gegenseitig verstärken: Die Chemotherapie kann Tumorzellen schädigen und dadurch für das Immunsystem „sichtbarer“ machen – und Durvalumab hilft dem Immunsystem dann, diese besser zu bekämpfen.
Nach der Chemotherapie wird Durvalumab als Erhaltungstherapie weitergegeben, um mögliche verbliebene Krebszellen langfristig unter Kontrolle zu halten und ein Rezidiv zu verhindern.
Endometriumkrebs kann unterschiedliche biologische Eigenschaften aufweisen. Eine wichtige Rolle spielt dabei, ob bestimmte Reparaturmechanismen in den Tumorzellen funktionsfähig sind oder nicht. Eine dieser Reparaturmechanismen nennt man Mismatch-Repair (MMR).
Wenn dieser Reparaturmechanismus nicht funktioniert, spricht man von dMMR (defizienter Mismatch-Repair). Solche Tumoren haben oft viele genetische Veränderungen und reagieren häufig besonders gut auf Immuntherapien wie Durvalumab.
Funktioniert das Reparatursystem dagegen normal, spricht man von pMMR (profizienter Mismatch-Repair). Diese Tumoren sind in der Regel weniger empfindlich gegenüber Immuntherapien, sodass hier zusätzliche Medikamente wie z. B. Olaparib eingesetzt werden, um die Wirkung zu verstärken.
Olaparib ist ein sogenannter PARP-Inhibitor, ein Medikament, das Krebszellen daran hindert, Schäden an ihrer DNA zu reparieren. Die Hinzunahme von Olaparib zur Durvalumab-Erhaltungstherapie bei pMMR-Tumoren kann helfen, das Tumorwachstum besser zu kontrollieren, indem er die Krebszellen anfälliger für eine Immunreaktion macht. Dieser Therapievorteil wurde in der Vergangenheit schon durch z. B. die DUO-E Studie gezeigt.
Ziel ist es, durch die kombinierte Erhaltungstherapie von Durvalumab + Olaparib auch bei Patientinnen mit pMMR-Tumoren eine möglichst wirksame und langfristige Kontrolle der Erkrankung zu erreichen.
Was ist das Ziel der Studie?
Im Zentrum der DUOLife-Studie steht die Frage, wie lange es dauert, bis die nächste Therapie nötig wird – ein Maß namens rwTTNT (real-world Time to Next Treatment). Außerdem wird unter anderem auch bewertet, wie lange die Erkrankung unter Kontrolle bleibt (rwPFS = real-world progressionsfreies Überleben), welche Nebenwirkungen aufgetreten sind und wie es den Patientinnen im Alltag geht (Lebensqualität, Symptome).
Wie ist der Ablauf der Studie?
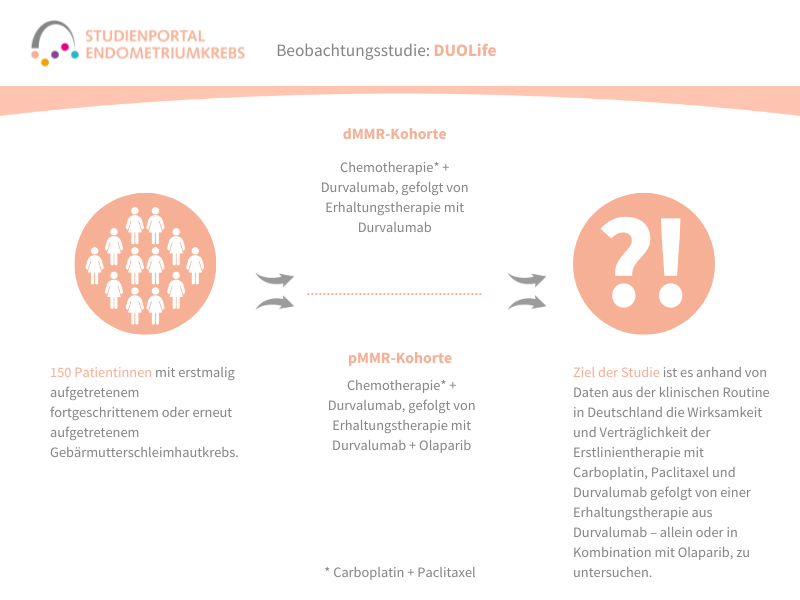
Insgesamt sollen rund 150 Patientinnen in Deutschland teilnehmen. Alle erhalten eine Therapie, die in der klinischen Routine bereits angewendet wird – es handelt sich also nicht um eine klinische Studie mit experimenteller Behandlung.
Bei jeder Patientin mit Endometriumkrebs wird bei Diagnose festgestellt, ob der Tumor dMMR oder pMMR ist. In Abhängigkeit von ihrer Diagnose können die Patientinnen in eine dieser beiden Gruppe eingeschlossen werden:
- dMMR-Kohorte: Patientinnen erhalten eine Chemotherapie in Kombination mit Durvalumab. Danach folgt eine Erhaltungstherapie mit Durvalumab
- pMMR-Kohorte: Patientinnen erhalten ebenfalls die Kombination aus Chemotherapie und Durvalumab, anschließend folgt eine Erhaltungstherapie mit Durvalumab plus Olaparib.
Für die Studie erfolgen keine zusätzlichen Untersuchungen oder Besuche am Studienzentrum über die reguläre Versorgung hinaus. Zusätzlich zu den Routineuntersuchungen werden Sie lediglich gebeten Fragebögen für die Auswertung der Lebensqualität zu beantworten.
Gibt es Risiken?
Es handelt sich um eine reine Beobachtungsstudie, d. h. die Patientinnen erhalten ihre geplante oder bereits begonnene Krebstherapie. Darüber hinaus bekommen sie keine zusätzlichen Medikamente oder andere Behandlungen (ausgenommen sind hier Medikationen für Begleiterkrankungen oder Medikationen gegen eventueller Nebenwirkung der Routinebehandlung). Die Risiken und Nebenwirkungen sind damit die gleichen, als würde die Behandlung außerhalb dieser Beobachtungsstudie stattfinden.
Teilnahmevoraussetzungen
An dieser Studie können Frauen im Alter ab 18 Jahren teilnehmen mit:
- Fortgeschrittenem (Stadium FIGO III oder IV) oder rezidiviertem Endometriumkrebs
- Bekanntem MMR-Status (genetische Eigenschaft des Tumors, die bei der Diagnose festgestellt wird: dMMR oder pMMR)
- Geplante oder bereits begonnene Erstlinientherapie mit einer Kombination aus Chemotherapie (Carboplatin + Paclitaxel, kurz CP) und Durvalumab
- Bereitschaft, regelmäßig Fragebögen zur Lebensqualität (sogenannte PROs – patient-reported outcomes) auszufüllen
Darüber hinaus gibt es aber auch noch weitere Kriterien, die für eine Teilnahme an der Studie erfüllt sein müssen. Weitere Informationen erhalten Sie über Ihre behandelnden Ärzt:innen.
Diese Studie wird unterstützt von:






