ENGOT-EN20 / XPORT-EC-042
THERAPIESTUDIE MIT SELINEXOR ALS ERHALTUNGSTHERAPIE NACH SYSTEMISCHER THERAPIE BEI PATIENTINNEN MIT P53-WILDTYP, FORTGESCHRITTENEM ODER REZIDIVIERENDEM ENDOMETRIUMKREBS
Die Rekrutierung in der XPORT Studie wurde im Januar 2026 beendet.
Die XPORT-EC-042 ist eine randomisierte (zufällige Zuteilung in die Behandlungsarme), Placebo-kontrollierte, doppelblinde (Ärzt:innen und Teilnehmerinnen wissen nicht, wer welchem Arm zugeteilt wurde) Phase-3-Studie mit Selinexor als Erhaltungstherapie nach systemischer Therapie bei Patientinnen mit fortgeschrittenem oder rezidivierendem Endometriumkrebs, ohne p53-Mutation im Tumorgewebe.
Was wird in dieser Studie untersucht?
Die derzeitige Standardtherapie für die Erstbehandlung von fortgeschrittenem oder rezidivierendem Endometriumkrebs ist die intravenöse Verabreichung von Carboplatin und Paclitaxel (Chemotherapie). Obwohl mehr als die Hälfte der Patientinnen auf die Behandlung anspricht, kommt es leider bei fast allen Patientinnen innerhalb kurzer Zeit zu einem Rezidiv (Rückkehr der Erkrankung). Deswegen wird aktuell nach einer Erhaltungstherapie gesucht, die das anfängliche Ansprechen des Tumors auf die Chemotherapie weiter unterstützt und das Wiederauftreten und/oder Fortschreiten der Krankheit durch die Beseitigung von Restkrebszellen verzögert. In bereits vorangegangenen Studien (SIGN und SIENDO) wurden erste Hinweise darauf gefunden, dass Selinexor die Krankheitskontrolle bei Patientinnen mit Endometriumkrebs verbessert. Die XPORT-Studie soll nun darauf aufbauen und die Wirksamkeit von Selinexor als Erhaltungstherapie bei Patientinnen mit Endometriumkarzinom ohne p53-Mutation genauer untersuchen.
Die SIGN-Studie war eine Phase-2-Studie zur Bewertung der Sicherheit und Wirksamkeit von Selinexor bei Patientinnen mit fortgeschrittenen gynäkologischen Malignomen. Die Ergebnisse belegen die Wirksamkeit des Medikaments bei Patientinnen mit stark vorbehandelten gynäkologischen Krebserkrankungen. Die SIENDO ist eine Studie mit Selinexor als Erhaltungstherapie im Vergleich zu Placebo nach einer Kombinations-Chemotherapie bei Patientinnen mit fortgeschrittenem oder wiedergekehrtem Endometriumkrebs. Eine Analyse der SIENDO-Daten zeigte, dass Patientinnen mit Endometriumkrebs ohne p53-Mutation eine bedeutsame Verbesserung durch die Selinexor-Erhaltungstherapie im Vergleich zu Placebo haben. Selinexor war in der SIENDO-Studie außerdem sicher und einigermaßen gut verträglich.
Selinexor ist ein selektiver Inhibitor, also ein Hemmstoff, der speziell ein bestimmtes Protein (Exportin-1) hemmt. Dieses Protein ist zuständig für den Transport von bestimmten Proteinen, Wachstumsregulatoren und Tumor-spezifischen mRNAs aus dem Zellkern heraus. Wird Exportin-1 gehemmt reichern sich diese Proteine im Zellkern an und können dafür sorgen, dass der Zelltod eintritt und somit das Tumorwachstum gehemmt wird.
Was ist das Ziel der Studie?
Das Hauptziel der Studie ist die Bewertung der Wirksamkeit von Selinexor als Erhaltungstherapie im Vergleich zu Placebo. Dafür wird das allgemeine Überleben und das progressionsfreie Überleben (das heißt von Beginn der Behandlung im Rahmen der Studie bis zum weiteren Fortschreiten der Erkrankung), zwischen den beiden Behandlungsarmen verglichen. Außerdem werden die Sicherheit und Verträglichkeit von Selinexor, sowie die Lebensqualität während der Behandlung bewertet.
Wie ist der Ablauf der Studie?
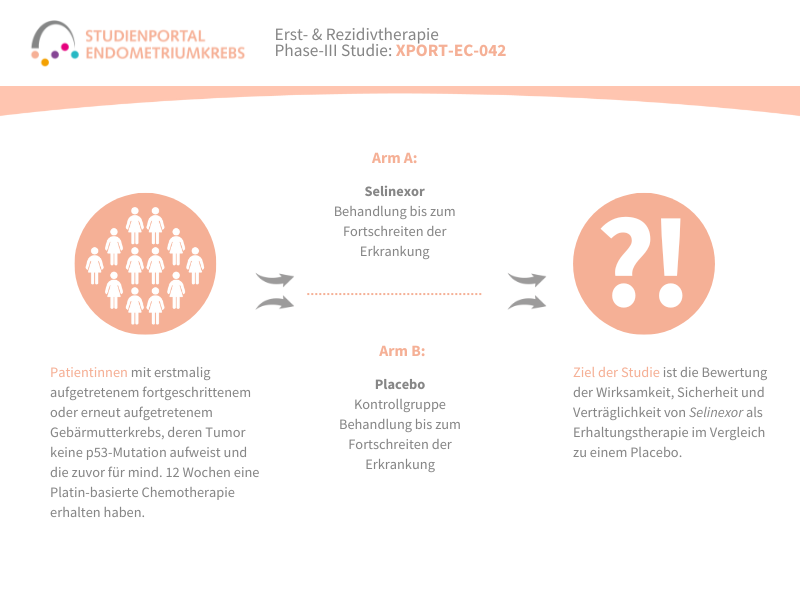
Die Patientinnen werden in einem Verhältnis von 1:1 zufällig einem der zwei Behandlungsarme zugeteilt:
Arm A: Selinexor
Arm B: Placebo
In beiden Behandlungsarmen erfolgt die medikamentöse Behandlung bis zum Fortschreiten der Erkrankung.
Gibt es Risiken?
Über mögliche Risiken bzw. Nebenwirkungen, die mit der Teilnahme verbunden sind, werden Sie im Rahmen eines Aufklärungsgesprächs von Ihrem Arzt bzw. Ihrer Ärztin informiert.
Teilnahmevoraussetzungen
An dieser Studie können Frauen im Alter ab 18 Jahren teilnehmen:
- mit neu bestätigter Diagnose von fortgeschrittenem (Stadium-IV) oder rezidiviertem Endometriumkrebs
- Tumor weist keine p53-Mutation auf
- Mindestens 12 Wochen Platin-basierte Chemotherapie als Vorbehandlung
Darüber hinaus gibt es aber auch noch weitere Kriterien, die für eine Teilnahme an der Studie erfüllt sein müssen. Weitere Informationen erhalten Sie über Ihre behandelnden Ärzt:innen.
Diese Studie wird unterstützt von:






